⭐️ Hầu hết các cơ sở y tế đều sử dụng các sản phẩm TTBYT sử dụng một lần sản xuất trong nước vì chất lượng sản phẩm trong nước ngày càng tốt, giá thành cạnh tranh. Những thiết bị công nghệ cao đã được một số bệnh viện sử dụng bên cạnh thiết bị nhập khẩu.
⭐️ Các doanh nghiệp đang phấn đấu áp dụng hệ thống quản lý chất lượng ISO 13485, cải tiến chất lượng, mẫu mã đáp ứng yêu cầu sử dụng, thị hiếu người dùng và vươn tới xuất khẩu.
I. Đối Tượng Áp Dụng ISO 13485:2016
✅
Tiêu chuẩn ISO 13485: được áp dụng cho tất cả tổ chức, không phân biệt loại hình, địa điểm, quy mô,... Có thể bao gồm: các cơ sở / công ty / nhà máy / nhà phân phối,... thực hiện sản xuất kinh doanh thiết bị y tế, dịch vụ y tế nói chung (ví dụ: Sản xuất Găng tay y tế, Dụng cụ tiệt trùng sản phẩm y tế, kim chích, dây truyền dịch, dây cho ăn,...)
✅ Tiêu chuẩn ISO 13485: mang tính chất tự nguyện, tập trung vào việc quản lý an toàn sản phẩm y tế. Khi tổ chức xây dựng và đáp ứng theo tiêu chuẩn ISO 13485, tổ chức có hệ thống quản lý an toàn có thể tạo ra môi trường làm việc giảm thiểu rủi ro liên quan tới an toàn sản phẩm thiết bị y tế, sản phẩm được tạo ra an toàn, nhằm thỏa mãn nhu cầu của khách hàng và yêu cầu luật pháp.
✅ Tổ chức có thể xây dựng hệ thống quản lý chất lượng ISO 13485 độc lập hoặc kết hợp với các hệ thống quản lý khác, Một số dịch Công bố Thiết bị y tế, Phân Loại thiết bị y tế,...
II. Quy Trình Hệ Thống Quản Lý ISO 13485:2016 - Đơn Vị Tư Vấn Độc Lập
Bước 1: Đơn vị tư vấn hướng dẫn thành lập ban ISO. Thành viên ban ISO do tổ chức chỉ định. Thông thường các thành viên là các trưởng phó bộ phận / phòng ban.
Bước 2: Đơn vị tư vấn tiến hành đào tạo cho thành viên ban ISO: Đào tạo nhận thức tiêu chuẩn, đào tạo yêu cầu tiêu chuẩn và hướng dẫn triển khai yêu cầu tiêu chuẩn.
Bước 3: Tư vấn trực tiếp hướng dẫn người được phân công soạn tài liệu theo yêu cầu của tiêu chuẩn phù hợp với tình hình thực tế của tổ chức. Trong quá trình tư vấn sẽ ảnh hưởng không nhiều đến công tác nghiệp vụ của người được phân công.
Bước 4: Tư vấn viên đến hướng dẫn bộ phận phụ trách ban hành quy trình thực hiện, ban hành và hướng dẫn các bộ phận liên quan áp dụng các quy trình đã ban hành.
Bước 5: Tư vấn tiếp tục hướng dẫn thành viên ban triển khai dự án kỹ thuật duy trì hệ thống. Đào tạo các thành viên trở thành đánh giá viên nội bộ của tổ chức giúp duy trì hệ thống cho tổ chức.
Bước 6: Các chuyên gia đánh giá đã từng có kinh nghiệm đánh giá cho các tổ chức chứng nhận thực hiện đánh giá. Các đánh giá viên nội bộ của tổ chức theo tập sự để học hỏi kỹ thuật và kinh nghiệm thực tế.
Bước 7: Tư vấn hướng dẫn trực tiếp người được phân công khắc phục điểm không phù hợp theo yêu cầu của tiêu chuẩn và yêu cầu của tài liệu đã soạn.
Bước 8: Chuyên gia đánh giá bên tư vấn đến quan sát và hỗ trợ các đánh giá viên đã học và tập sự triển khai đánh giá nội bộ chính thức. Đơn vị tư vấn hướng dẫn khắc phục theo yêu cầu của tiêu chuẩn và yêu cầu của tài liệu đã soạn.
Bước 9: Tư vấn hướng dẫn tổ chức đăng ký chứng nhận ISO 13485:2016 với tổ chức chứng nhận có đủ năng lực pháp lý.
Tư vấn viên quản lý dự án sẽ tham gia hỗ trợ tổ chức khi đơn vị chứng nhận đến đánh giá.
Bước 10: Sau khi được đánh giá chứng nhận, nếu tổ chức còn tồn tại điểm không phù hợp, đơn vị tư vấn sẽ hỗ trợ khắc phục để đáp ứng yêu cầu tiêu chuẩn và yêu cầu của đơn vị chứng nhận.
Bước 11: Sau khi có kết quả thẩm xét của đơn vị chứng nhận. Nếu đánh giá đạt, đơn vị chứng nhận sẽ cấp giấy chứng nhận ISO 13485 cho tổ chức. Giấy chứng nhận ISO 13485 thường có hiệu lực trong 3 năm, mỗi năm đơn vị chứng nhận sẽ tiến hành đánh giá giám sát hệ thống quản lý ISO 13485 để duy trì hiệu lực chứng chỉ.
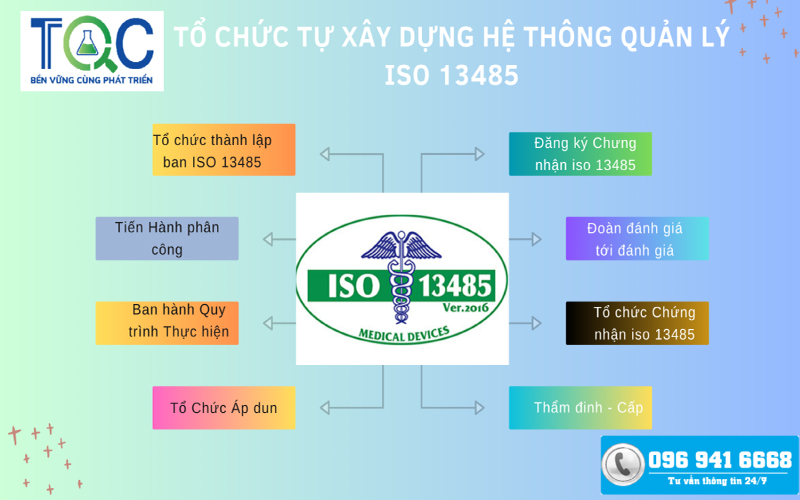
III. Quy Trình Triển Khai Hệ Thống Quản Lý ISO 134585:2016 - Tổ Chức Tự Xây Dựng Hệ Thống Quản Lý
Bước 1: Tổ chức thành lập ban ISO. Thành viên ban ISO do tổ chức chỉ định. Thông thường các thành viên là các trưởng phó bộ phận/phòng ban.
Bước 2: Ban ISO tiến hành phân công xây dựng, soạn tài liệu theo yêu cầu của tiêu chuẩn phù hợp với tình hình thực tế của tổ chức. Người phân công thường là trưởng ban ISO, có chứng nhận chuyên gia đánh giá trưởng cho hệ thống quản lý ISO 13485:2016.
Bước 3: Ban ISO và các bộ phận phụ trách ban hành quy trình thực hiện, ban hành và hướng dẫn các bộ phận liên quan áp dụng các quy trình đã ban hành.
Bước 4: Tổ chức tiến hành áp dụng các quy trình thực hiện đã ban hành, tiến hành kiểm soát nội bộ đồng thời cải tiến hệ thống nhằm đáp ứng đúng các yêu cầu trong tiêu chuẩn ISO 13485.
Bước 5: Sau quá trình áp dụng và cải tiến, tổ chức có thể đăng ký chứng nhận ISO 13485 với các đơn vị chứng nhận uy tín để được đánh giá và cấp chứng nhận theo quy định.
Bước 6: Đoàn đánh giá chứng nhận tới đánh giá chính thức sau khi đánh giá, thẩm tra tài liệu sơ bộ.
Bước 7: Tổ chức nhận kết quả đánh giá và tiến hành khắc phục các điểm không phù hợp so với tiêu chuẩn và quy trình thực hiện đã ban hành (nếu có) được chuyên gia đánh giá chỉ ra sau quá trình đánh giá hệ thống quản lý của tổ chức.
Bước 8: Sau khi có kết quả thẩm xét của đơn vị chứng nhận. Nếu đánh giá đạt, đơn vị chứng nhận sẽ cấp giấy chứng nhận hệ thống quản lý ISO 13485 cho tổ chức. Giấy chứng nhận ISO 13485 thường có hiệu lực trong 3 năm, mỗi năm đơn vị chứng nhận sẽ tiến hành đánh giá giám sát hệ thống quản lý ISO 13485 để duy trì hiệu lực chứng chỉ.
IV. Lợi Ích Khi Áp Dụng Hệ Thống Quản Lý ISO 13485:2016
Lĩnh vực Chứng nhận Thiết bị Y tế
► Hiện nay, lĩnh vực TBYT có 15.000 chủng loại mặt hàng, mỗi sản phẩm lại có mức rủi ro khác nhau, không có giới hạn về nguyên vật liệu sản xuất hay chỉ định mục đích sử dụng. Do vậy, để quản lý tốt TTBYT đòi hỏi phải phân loại rõ ràng về mức độ rủi ro trên cơ sở xây dựng danh mục TTBYT.
► Thường xuyên được cập nhật, vừa đảm bảo tính khả thi vừa thuận lợi cho doanh nghiệp, tăng cường quản lý nhà nước về TTBYT. Các doanh nghiệp sản xuất cũng cần đáp ứng yêu cầu ISO 13485 để nâng cao năng lực đồng thời đảm bảo yêu cầu pháp lý.
Sản phẩm TBYT
►Các TTBYT sản xuất trong nước tập trung vào các sản phẩm sử dụng một lần, nội thất bệnh viện, thiết bị tiệt trùng, trang thiết bị y tế IVD, dịch lọc thận gel siêu âm, máy vật lý trị liệu, máy điện châm, đo huyết áp, trợ thính, công nghệ cao, khí y tế...
► Các cơ sở sản xuất có thể áp dụng và duy trì hệ thống quản lý theo ISO 13485 sẽ có thể duy trì chất lượng ổn định, theo thời gian cải tiến hệ thống sẽ dần nâng cao chất lượng, đủ khả năng cạnh tranh với các sản phẩm nhập khẩu. Ngoài ra việc áp dụng ISO 13485 còn cung cấp phương tiện để thực hiện công việc đúng ngay từ đầu, giảm hư hỏng, giảm lãng phí;
►Giải phóng được công việc mang tính chất tập trung sự vụ của lãnh đạo. Giúp lãnh đạo doanh nghiệp có nhiều thời gian tập trung vào thực hiện chiến lược mang tầm vĩ mô hơn...
Dịch vụ Chứng nhận ISO 13485:2016 - Hệ thống quản lý chất lượng Thiết bị y tế: Uy Tín - Nhanh Chóng
✅ Đạt Giấy chứng nhận ISO 13485.
✅ Chi phí Chứng nhận đạt tiêu chuẩn ISO 13485:2016 tối ưu.
✅ Quy trình làm việc chuyên nghiệp, hiệu quả.
✅ Thuận tiện Văn phòng có 3 miền.
✅ Hơn 100+ Chuyên gia đầu ngành.
V. Trung Tâm TQC – Đơn Vị Chứng Nhận ISO 13485:2016 Uy Tín
Thông tin Chỉ định và thông tin Chứng nhận iso 13485:2016
-
TQC là tổ chức khoa học công nghệ được Bộ Khoa học và công nghệ cấp Đăng ký hoạt động. TQC luôn đặt chất lượng dịch vụ chứng nhận và yếu tố đúng hẹn lên hàng đầu.
-
Khi sử dụng dịch vụ, khách hàng sẽ luôn được TQC song hành, hỗ trợ tối đa và đầy đủ các bước thực hiện, đảm bảo thuận lợi trong quá trình hoàn thiện thủ tục, đăng ký, đánh giá và tiếp nhận Giấy chứng nhận.
-
Bằng năng lực chuyên sâu cùng uy tín của mình, TQC được nhiều khách hàng, đối tác tin tưởng lựa chọn là đơn vị chứng nhận hệ thống quản lý, đồng hành cùng doanh nghiệp trong quá trình xây dựng và hoàn thiện hệ thống quản lý chất lượng ISO 13485.
-
Một số doanh nghiệp tiêu biểu sản xuất thiết bị y tế như: Dược phẩm Nhất Nhất, Công ty cổ phẩn Dược - Thiết bị y tế Đà Nẵng - DAPHARCO, dược phẩm Quang Minh, OPODIS Pharma, Công ty cổ phần giải pháp Gene (Gene Solutions),...
-
Ngoài 3 văn phòng đại diện tại Hà Nội, Đà Nẵng và Tp.Hồ Chí Minh thì Trung tâm TQC còn có mạng lưới chuyên gia giàu kinh nghiệm có mặt tại rộng khắp các tỉnh thành trên cả nước.TQC có Văn phòng Campuchia, Văn phòng ở Hoa kỳ.

✔ TQC triển khai đi đầu về cung cấp Dịch vụ Đào tạo Chứng nhận iso 13485- Hệ Thống quản lý chất lượng trang thiết bị y tế
✔ TQC có hơn 15 năm kinh nghiệm trong lĩnh vực chứng nhận, Đào tạo đăng ký quy mô trên 100 nhân sự, 5 văn phòng trải rộng trên cả nước và đối tác liên kết toàn cầu tại 5 thị trường lớn: Hoa Kỳ, Châu âu, Trung Quốc, Ấn Độ, Nhật Bản.
✔ Văn phòng có mặt tại 03 miền.
✔ Với hơn 4000 khách hàng đã sử dụng dịch vụ.
✔ Quy trình làm việc khoa học, nhanh chóng - uy tín.
✔ Dịch vụ trọn gói, không phát sinh chi phí.